ПРЕДЕЛЬНЫЕ, ИЛИ НАСЫЩЕННЫЕ, УГЛЕВОДОРОДЫ РЯДА МЕТАНА (АЛКАНЫ, ИЛИ ПАРАФИНЫ)
Алканы, или парафины — алифатические предельные углеводороды, в молекулах которых атомы углерода связаны между собой простой (одинарной) (s-связью.
Оставшиеся валентности углеродного атома, не затраченные на связь с другими атомами углерода, полностью насыщены водородом. Поэтому предельные (насыщенные) углеводороды содержат в молекуле максимальное число водородных атомов.
1.1. СТРОЕНИЕ АЛКАНОВ
Простейшим представителем и родоначальником предельных углеводородов является метан СН4. Строение молекулы метана можно выразить структурной (I) или электронной (II) формулой:
H|H—C—H|H(I) |
H ..H :C : H..H(II) |
В предельных углеводородах атомы углерода находятся в первом валентном состоянии (sp3-гибpидизaция). В этом случае, .как известно, все четыре гибридные орбитали в пространстве составляют геометрическую фигуру — тетраэдр (углы между осями связей С—Н равны 109° 28'). Пространственное расположение атомов в молекуле метана можно показать с помощью тетраэдрических и шаростержневых моделей (рис. 1). Для этого наиболее удобны объемные модели Бриглеба, которые более наглядно отражают относительные размеры атомов в молекуле. Эти модели изготовлены в соответствии с действительным соотношением радиусов атомов (в масштабе 0,05 нм = 1 см).

Рис.1. Модели пространственного строения молекулы метана:
а - тетраэдрическая; б - шаростержневая; в - по Бриглебу
Если в молекуле метана один атом водорода заместить на метильную группу СН3, то можно вывести структурную формулу следующего за метаном углеводорода — этана C2H6:
H H| |H—C—C—H| |H H |
или H3C—CH3 |
Замещая в молекуле этана один атом водорода на метальную группу, выводим формулу третьего углеводорода — пропана С3Н8:
H H H| | |H—C—C—С—H| | |H H H |
или H3C—CH2—CH3 |
Повторяя это действие много раз, можно вывести формулы и других предельных углеводородов, отличающихся друг от друга числом углеродных атомов (табл. 1). В результате образуется ряд соединений, в котором каждый член отличается от предыдущего на одну группу СН2. Такой ряд называется гомологическим рядом (от греч. homos — последовательный), а его отдельные члены — гомологами. Они обладают близкими химическими свойствами и закономерным изменением физических свойств. Из табл. 1 видно, что у каждого члена гомологического ряда на п атомов углерода приходится 2n + 2 атомов водорода. Следовательно, состав любого члена этого ряда будет выражаться общей формулой СnН2n + 2. Используя эту формулу, можно легко написать молекулярную формулу любого предельного углеводорода — алкана, зная число углеродных атомов в его молекуле. Например, если п = 25, то углерод будет выражаться формулой C25H52.
Таблица 1. Гомологический ряд предельных углеводородов (алканов) нормального (неразветвленного) строения и их одновалентные радикалы
Углеводород (алкан) |
Число возможныхизомеров у алкана |
Радикал (алкил) |
||
Формула |
Название |
Формула |
Название |
|
СН4 |
Метан |
1 |
СН3- |
Метил |
С2Н6 |
Этан |
1 |
С2Н5- |
Этил |
С3Н8 |
Пропан |
1 |
С3Н7- |
Пропил |
С4Н10 |
Бутан |
2 |
С4Н9- |
Бутил |
С5Н12 |
Пентан |
3 |
С5Н11- |
Пентил |
С6Н14 |
Гексан |
5 |
С6Н13- |
Гексил |
C7H16 |
Гептан |
9 |
C7H15- |
Гептил |
C8H18 |
Октан |
18 |
C8H17- |
Октил |
С9Н20 |
Нонан |
35 |
С9Н19- |
Нонил |
С10Н22 |
Декан |
75 |
С10Н21- |
Децил (декил) |
Гомологические ряды характерны для всех классов органических соединений. Они являются прекрасным подтверждением основного закона природы — перехода количественных изменений в качественные.
Если от алкана "отнять" один атом водорода, то образуется одновалентный углеводородный остаток — радикал (не смешивайте с реально существующим свободным радикалом). При потере двух или трех атомов водорода образуются соответственно двух- или трехвалентные радикалы (табл. 2).
Таблица 2. Наиболее часто встречающиеся углеводородные радикалы
Название |
Формула радикала |
Название |
Формула радикала |
Метил |
СН3— |
Этил |
CH3—CH2— |
Метилен |
СН2== |
Этилиден |
CH3—CH== |
Метин |
СНєє |
Этилидин |
CH3—Cєє |
н-Пропил |
CH3—CH2—CH2— |
Изобутил (первичный изобутил) |
(СН3)2СН—СН2— |
Пропилиден |
CH3—CH2—CH== |
втор-Бутил |
CH3 |CH3—CH2—CH— |
Изопропил |
(СН3)2СН— |
терет-Бутил |
(СН3)3С— |
н-Бутил |
CH3—CH2—CH2—CH2— |
н-Пентил |
CH3—CH2—CH2—CH2—CH2— |
В приведенных названиях радикалов используют обозначения: н-нормальный, втор- — вторичный, трет- — третичный.
Как видно из табл. 2, свободная валентность в радикале может находиться при разных углеродных атомах. Если свободная валентность в радикале находится у первичного атома углерода, то такой радикал называется первичным. Соответственно этому могут быть вторичные (свободная валентность принадлежит вторичному атому углерода) и третичные (свободная валентность у третичного углеродного атома) радикалы:.
Н3С— - первичный одновалентный радикал (метил);
(СН3)2СН— - вторичный одновалентный радикал (изопропил);
(СН3)3С— - третичный одновалентный радикал (mpem-бутил).
1.2. НОМЕНКЛАТУРА И ИЗОМЕРИЯ
Номенклатура. Для названия предельных углеводородов применяют в основном систематическую и рациональную номенклатуры.
Названия первых четырех членов гомологического ряда метана тривиальные: метан, этан, пропан, бутан. Начиная с пятого названия образованы от греческих числительных с добавлением суффикса –ан (этим подчеркивается сходство всех предельных углеводородов с родоначальником этого ряда — метаном).
Общее (родовое) название предельных углеводородов — алканы. Названия по систематической номенклатуре составляют следующим образом:
- В формуле молекулы алкана выбирают главную цепь — самую длинную.
- Затем эту цепь нумеруют с того конца, к которому ближе расположен заместитель (радикал). Если заместителей несколько, то поступают так, чтобы цифры, указывающие их положение, были наименьшими. Заместители перечисляют по алфавиту.
| H3C—CH—CH2—CH—CH2—CH3 -------- | ----------- | CH3 ¦ CH2—CH2—CH3 --------------------- |
| 1
2 3
4 H3C—CH—CH2—CH—CH2—CH3 | 5 | 6 7 CH3 CH2—CH2—CH3 |
3. Углеводород называют в таком порядке: вначале указывают (цифрой) место расположения заместителя, затем называют этот заместитель (радикал), а в конце добавляют название главной (самой длинной) цепи. Таким образом, углеводород может быть назван: 2-метил-4-этилгептан (но не 6-метил-4-этилгептан).
Если в главной цепи содержится несколько одинаковых заместителей, то их число обозначают греческим числительным, которое ставят перед названием этих заместителей. Приставки ди-, три-, тетра- и т.д. не влияют на алфавитное расположение заместителей в названии.
Для простейших углеводородов изостроения сохраняются их несистематические названия: изобутан, изопентан, неопентад.
По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода — метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти заместители (радикалы) называют по старшинству (от менее сложных к более сложным). Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово "метан":
CH3|H3C—C—CH3|CH3 |
C2H5 | H3C—CH—CH—CH3|CH3 |
| тетраметилметан (2,2-диметилпропан) | метилэтилизопропилметан (2,3-диметилпентан) |
Свою номенклатуру имеют и радикалы (углеводородные радикалы). Одновалентные радикалы называют алкилами и обозначают буквой R или Alk. Их общая формула CnH2n + 1. Названия радикалов составляют из названий соответствующих углеводородов заменой суффикса -ан на суффикс -ил (метан — метил, этан — этил, пропан — пропил и т.д.). Двухвалентные радикалы называют, заменяя суффикс -ан на -илиден (исключение — радикал метилен ==СН2). Трехвалентные радикалы имеют суффикс -илидин (исключение — радикал метин єєСН).
Изомерия.
Для алканов характерен самый простой вид изомерии — структурная изомерия.
В молекулах метана, этана и пропана может быть только один порядок соединения атомов.
Если в молекуле алкана содержится более трех углеродных атомов, то порядок их соединения может быть различным — появляется возможность изомерии. Например, для углеводорода С4Н10 возможны две структуры:
H H H H| | | |H—C—C—С—С—H| | | |H H H H |
H H H | | |H—C—C—С—H| | |H | HH—C—H|H |
н-бутан (н-C4H10) |
изобутан (изо-С4Н10) |
Один из этих изомеров (н-бутан) содержит неразветвленную углеродную цепь, а другой — изобутан — разветвленную (изостроение). Таким образом, молекулы бутана и изобутана, имея одинаковый состав, различаются между собой химическим строением, т.е. они являются структурными изомерами. Изомеры обладают сходными химическими свойствами и различными — физическими.
Атомы углерода в алканах могут различаться по характеру своего соединения с другими углеродными атомами. Атом углерода, связанный только с одним углеродным атомом, называется первичным, с двумя — вторичным, с тремя — третичным и, наконец, с четырьмя — четвертичным. Это можно пояснить на примере:
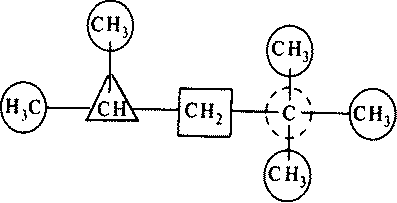
2,2,4-триметилпентан
Здесь первичные углеродные атомы обведены кружком, вторичный — квадратом, третичный — треугольником, четвертичный — пунктирным кружком.
Такое деление имеет большое значение, так как водородные атомы при первичном, вторичном и третичном углеродных атомах обладают различной реакционной способностью.
В ряду радикалов мы также встречаемся с явлением изомерии (см. табл. 2). Причем число изомеров у радикалов значительно больше, чем у соответствующих им алканов. Например, пропан, как известно, изомеров не имеет, а радикал пропил имеет два изомера: н-пропил и изо-пропил:
|
СН3—СН3—СН2— и Н3С—СН—СН3
Это связано с тем, что свободная валентность может находиться при разных углеродных атомах (вторичном и третичном).
1.3. ПОЛУЧЕНИЕ АЛКАНОВ
Для получения алканов используют в основном природные источники. Газообразные алканы получают из природного и попутных нефтяных газов, а твердые алканы — из нефти. Природной смесью твердых высокомолекулярных алканов является горный воск (озокерит) — разновидность твердого природного битума.
Многие предельные углеводороды можно получать методом гидрирования углей:
500 °С
nC + 2nН2 ®
СnН2n + 2
оксиды железа
Так как при этом из твердого угля образуется смесь жидких продуктов, процесс называется сжижением угля.
С этой же целью используют смесь оксида углерода и водорода (синтез-газ) в присутствии катализатора (кобальта или никеля):
200 °С
nCО + (2n + 1)Н2 ® СnН2n
+ 2 + n Н2О
кат.
Образующиеся алканы находят применение в качестве моторного топлива (синтетический бензин — "синтин").
Для получения алканов часто применяют лабораторные методы - органический синтез.
1. Гидрирование этиленовых и ацетиленовых углеводородов в присутствии катализатора (Pt, Pd, Ni):
Pt
Pt
H2C==CH2 + H2 ® H3C—CH3
H—CєєC—H + 2H2 ® H3C—CH3
этилен
этан
ацетилен
этан
2. Действие металлического натрия на галогенопроизводные алканов (галогеналкилы) — реакция французского химика А.Вюрца:
Н3С—I + 2Na + I—СН3 ® Н3С—СН3 + 2NaI
йодистый метил
Этот синтез служит для получения алканов из однородных галогеналкилов. Если в реакцию вводят два различных галогеналкила, то образуется не один продукт, а их смесь. Например:
Н3С—I + 2Na + I—С2Н5 ® Н3С—С2Н5 + 2NaI
пропан
Н5С2—I + 2Na + I—С2Н5 ® Н5С2—С2Н5 + 2NaI
бутан
3. Сплавление солей карбоновых кислот со щелочами:
Н3С—СOONa + NaOH ® СН4 + Na2CО3
4. Восстановление галогенопроизводных:
Pt
Н3С—С1 + Н2 ® CH4 + НС1
хлористый метил
1.4. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Физические свойства. Первые четыре члена гомологического ряда метана — газообразные вещества, начиная с пентана — жидкости, а углеводороды с числом углеродных атомов 16 и выше — твердые вещества (при обычной температуре). Температура кипения алканов с разветвленной цепью ниже, чем соединений нормального строения (табл. 3).
Алканы — неполярные соединения и трудно поляризуемые. Они легче воды и в ней практически не растворяются. Не растворяются также в других растворителях с высокой полярностью. Жидкие алканы — хорошие растворители для многих органических веществ.
Метан и этан, а также высшие алканы не имеют запаха, но среди других легколетучих низших углеводородов встречаются соединения, обладающие слабым запахом.
Алканы — горючие вещества. Метан горит бесцветным пламенем.
Таблица 3. Физические свойства алканов
Название |
Формула |
tпл °С |
tкип °С |
d204 |
Метан |
СН4 |
-182,5 |
-161,5 |
0,4150 (при -164 °С) |
Этан |
С2Н6 |
-182,8 |
-88,6 |
0,5610 (при -100 °С) |
Пропан |
С3Н8 |
-187,7 |
-42 |
0,5853 (при -44,5 °С) |
Бутан |
С4Н10 |
-138,3 |
-0,5 |
0,6000 (при 0°С) |
Пентан |
C5H12 |
-129,7 |
+36,1 |
0,6262 |
Гексан |
С6Н14 |
-95,3 |
68,7 |
0,6594 |
Гептан |
С7H16 |
-90,6 |
98,4 |
0,6838 |
Октан |
C8H18 |
-56,8 |
124,7 |
0,7025 |
Нонан |
С9Н20 |
-53,7 |
150,8 |
0,7176 |
Декан |
C10H22 |
-29,6 |
174,0 |
0,7300 |
Пентадекан |
C15H32 |
+10 |
270,6 |
0,7683 |
Эйкозан |
С20Н42 |
36,8 |
342,7 |
0,7780 (при 37 °С) |
Пентакозан |
C25H52 |
53,7 |
400 |
0,8012 |
Триаконтан |
С30Н62 |
66,1 |
457 |
0,8097 |
Химические свойства.
В алканах все атомы связаны между собой прочными (s-связями, а валентности углеродных атомов полностью насыщены водородом. Поэтому алканы не вступают в реакции присоединения. При обычных условиях они проявляют высокую химическую устойчивость. По этой причине алканы в свое время получили название парафинов (от лат. parum affinis — мало деятельный, мало сродства).
Основные химические превращения алканов идут только при сообщении им достаточно высокой энергии (при нагревании или облучении УФ-светом). При этом может произойти или разрыв связи С—Н с последующим замещением атома водорода на другой атом или группу атомов, или же разрыв молекулы по связи С—С. Несмотря на то что энергии этих связей равны соответственно 415-420 (для первичных углеродных атомов) и 350 кДж/моль, разрыв предпочтительнее идет по связи С—Н. Это связано с тем, что связь С—Н более доступна для реагента.
Поскольку алканы — соединения неполярные, то при разрыве связей образуются главным образом не ионы, а радикалы, т.е. этот процесс идет по гомолитическому механизму.
Таким образом, для алканов различают два основных типа химических реакций:
- реакции замещения водорода (с разрывом связи С—Н);
- реакции расщепления (с разрывом связей С—С и С—Н).
Реакции замещения. В этих реакциях замещение водорода легче происходит при третичном углеродном атоме, труднее — при вторичном и совсем плохо — при первичном.
1. Галогепирование (замещение галогеном) - важнейшая реакция алканов. Она протекает при освещении УФ-светом или в темноте при сильном нагревании, а также в присутствии катализаторов. Сравнительно легко алканы вступают в реакцию замещения с хлором и бромом, очень трудно — с иодом. С фтором реакция протекает со взрывом (поэтому обычно фтор разбавляют азотом или используют растворители). В результате замещения водорода галогеном образуются галогено-производные алканов. Например, хлорирование метана протекает с последовательным замещением в его молекуле всех атомов водорода на хлор:
СН4 + Cl2 ® СН3С1+ НС1
хлорметан
СН3С1 + Cl2 ® СН2С12 + НС1
дихлорметан
СН2С12 + Cl2 ® СНС13+ НС1
трихлорметан
СНС13 + Cl2 ® СС14 + НС1
тетрахлорметан
Реакция галогенирования имеет цепной свободно-радикальный характер (Н.Н.Семенов). На первой стадии этого процесса под влиянием УФ-облучения (или высокой температуры) происходит распад молекулы хлора на два свободных радикала. Такой процесс называется инициированием:
Сl : Сl ® С1Ч + С1Ч
Затем начинается рост цепи. Свободный радикал взаимодействует с молекулой метана:
СН4 + С1Ч ® СН3Ч + НС1
СН3Ч + Cl2 ® СН3Сl + С1Ч и т.д.
Эта реакция обрывается, если исчезнут свободные радикалы. Поэтому обрыв цепи часто связан с взаимодействием свободных радикалов друг с другом:
СН3Ч + СН3Ч ® Н3С:СН3
этан
С1Ч + С1Ч ® С1:С1
хлор
СН3Ч + С1Ч ® СН3:С1
хлорметан
2. Нитрование (замещение нитрогруппой NO2). Впервые эту реакцию открыл русский ученый М.И.Коновалов в 1888 г. (с тех пор она названа его именем). Алканы взаимодействуют с разбавленной азотной кислотой при нагревании, образуя нитропроизводные алканов:
Н3С—СН2—СН3 + HNO3 ® Н3С—СН—СН3
+ H2O
|
NO2
2-нитропропан
В промышленности реакцию нитрования проводят, нагревая алканы с парами азотной кислоты при 250—500 °С и давлении (парофазное нитрование). Реакция нитрования, как и галогенирования, идет по цепному радикальному механизму. Нитрующим агентом является радикалоподобный оксид азота NO2, который, взаимодействуя с алканом, образует свободный радикал — алкил RЧ:
R—H + NO2Ч ® RЧ + HNO2
Взаимодействие этих радикалов приводит к образованию нитросоединений:
RЧ + NO2Ч ® R—NO2
3. Сульфирование. Дымящая серная кислота (содержащая растворенный в ней SO3) с высшими алканами дает сульфокислоты. Например:
С17Н36 + H2SO4
® С17Н35SО3Н + Н2O
гептадекан
гептадецил-
сульфокислота
В результате таких реакций атом водорода в молекуле алкана замещается на сульфогруппу - SO3Н.
Соли сульфокислот (алкилсульфонаты) с C12-18 широко используются в качестве моющих средств. Эти соли можно получить и реакцией сульфохлорирования — действием на алканы смесью диоксида серы и хлора:
С10Н22 + SO2
+ Cl2 ® C10H21SO2Cl
+ HC1
Декан
сульфохлорид
декана
При взаимодействии сульфохлорида со щелочью образуется алкилсульфонат:
C10H21SO2Cl + 2NaOH ® C10H21SO3Na + NaCI + H2O
Реакции расщепления протекают при нагревании (в присутствии катализаторов или без них).
1. Отщепление водорода {дегидрирование). При нагревании алканов присутствии катализатора (СrО3) происходит отщепление атомов водорода с образованием непредельных углеводородов:
t
Н3С—СН2—СН3 ® Н2С==СН—СН3
пропан
-H2
пропилен
2. Термическое разложение (разрыв связей С—С и С—Н). Известно, что алканы устойчивы только при сравнительно невысоких температурах. При нагревании алканов до 500 ° С и выше, (без катализаторов или в их присутствии) они разлагаются с разрывом связей С—С и С—Н. В результате происходит образование более простых углеводородов — предельных и непредельных. Этот процесс называют крекингом.
3. Изомеризация. При этой реакции неразветвленная углеродная цепь превращается в разветвленную. Это сопровождается разрывом связей С—С:
Процесс изомеризации проходит при нагревании в присутствии катализатора (А1С13). В эту реакцию вступают только те алканы, которые в углеродной цепи содержат не менее четырех углеродных атомов.
Реакции окисления.
При обычных условиях алканы устойчивы к действию даже сильных окислителей (КМnO4, К2СrO4 и др.). Поэтому при добавлении к алканам водного раствора перманганата калия окраска раствора не меняется. Однако при каталитическом окислении (в присутствии солей марганца) и одновременном нагревании происходит окисление алканов (особенно высших) с образование многих кислородсодержащих веществ (спиртов, кетонов, карбоновых кислот и др.).
Основным способом переработки метана является его конверсия окисление водяным паром, кислородом или оксидом углерода (IV) присутствии катализатора и при высокой температуре:
СН4 + H2O ® CO + 3H2
CH4 + 1/2O2 ® CO + 2H2
CH4 + CO2 ® 2CO + 2H2
В результате этих реакций образуется синтез-газ (водяной газ) — ценное сырье для получения многих органических соединений (углеводородов, метилового и других спиртов и т.д.).
На воздухе алканы горят с образованием оксида углерода (IV) и воды. Например:
СН4 + 2O2 ® СO2 + 2Н2O
При этом выделяется значительное количество теплоты.
1.5. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ
Метан СН4 является главной составной частью природных (до 98 %) и попутных газов. В значительных количествах он присутствует в газах нефтепереработки. Метан используют в основном в качестве дешевого топлива в промышленности и быту.
Метан — бесцветный газ, без запаха. Для обнаружения его утечки в газопроводах используют некоторые сильно пахнущие вещества (одоранты), например низшие тиоспирты. В смеси с воздухом метан взрывоопасен.
Метан является ценным сырьем для химической промышленности. Из него получают ацетилен, галогенопроизводные, метанол, формальдегид и другие вещества. Метан служит для производства синтез-газа, газовой сажи:
СН4 + O2 ® С + 2Н2O
Этан С2H6, пропан С3Н8, бутан С4Н10 и пентан C5H12 применяют для получения соответственно этилена, пропилена, дивинила и изопрена. Пропан в смеси с бутаном используют в качестве топлива (бытовой сжиженный газ, транспортируемый в баллонах).
Изооктан C8H18 (2,2,4-триметилпентан) — ценная составная часть высококачественного горючего (бензина) для двигателей внутреннего сгорания:
СH3
|
H3C—C—CH2—CH—CH3
|
|
CH3
CH3
Моторное топливо должно обладать максимальной устойчивостью к детонации. В двигателях внутреннего сгорания детонация вызывается преждевременным воспламенением горючей смеси. Наименее детонируют разветвленные углеводороды, например такие, как изооктан. Его стойкость к детонации принята за 100 (н-гептан, наоборот, за 0). Поэтому качество бензинов характеризуют "октановым числом" (например, 76; 93 и др.). Для повышения детонационной стойкости бензина к нему добавляют антидетонаторы (тетраэтилсвинец и др.).
Средние члены гомологического ряда метана (C7 – C17) используют как растворители и моторное топливо.
Высшие алканы (C18 - С44) применяют для производства высших кислот и спиртов, синтетических жиров, смазочных масел, пластификаторов и непредельных соединений.
Поддержите сайт, поставте на нас ссылку. | |
| Пример ссылки | Код ссылки |
| Мир химии | |
| Выбрать другой баннер... | |




