Углерод
Получим диоксид углерода
Диоксид углерода можно получить из солей угольной кислоты (карбонатов), если вытеснить его с помощью более сильных кислот. В технике его получают при обжиге извести, т. е. В результате нагревания известняка при температуре примерно 1000 °C
СаСО3 = СаО + СО2
В лабораторных условиях применим самый дешевый способ. Для этого в аппарате для получения газов, например в аппарате Киппа, зальем кусочки мрамора (карбоната кальция СаСО3) 20%-ным раствором соляной кислоты:
СаСО3 + 2HCl = СаСl2 + H2O + СO2
Само собой разумеется, что пригодны и другие карбонаты: сода (карбонат натрия Na2CQ3), поташ (карбонат калия K2CO3), питьевая сода (гидрокарбонат натрия NаНСО3), и ряд кислот, в том числе даже относительно слабые — уксусная, винная и лимонная.
Полученный в аппарате диоксид углерода уловим в пневматической ванне или лучше вытеснением воздуха. Диоксид углерода тяжелее воздуха, 1 л его при 0°С и 760 мм рт. ст. весит 1,977 г, поэтому им можно наполнить стоячий сосуд, опустив газоотводную трубку на самое дно сосуда. Так как горящая лучина гаснет в атмосфере углекислого газа, то таким образом можно .проверить, наполнился ли наш сосуд.
Есть простое правило, которое помогает узнать, легче газ воздуха или тяжелее. Условимся число 29 считать относительной молекулярной массой воздуха и сравним молекулярные массы (М) газов с этой величиной. Например, молекулярная масса метана СН4 16, значит, метан легче воздуха; для азота N2 М = 28, т. е. азот немного легче воздуха, a SО2 (M = 64) и СО2 {М = 44) значительно тяжелее воздуха.
Опыты с диоксидом углерода
Диоксид углерода образует при взаимодействии с известковой водой осадок карбоната кальция, который при дальнейшем действии газа переходит в растворимый гидрокарбонат кальция:
Са(ОН)2 + СО2 = СаСО3 + Н2О
СаСО3 + Н2О + СО2 = Са(НСО3)
Для того чтобы получить известковую воду, зальем водой в химическом стакане негашеную или гашеную известь (защитить глаза!) и профильтруем отстоенный раствор или бросим кусочек карбида кальция в химический стакан с водой и после прекращения выделения газа профильтруем раствор.
Даже незначительные количества солей угольной кислоты можно обнаружить с помощью следующей пробы: в маленькую пробирку введем несколько частичек карбоната и 2 капли соляной кислоты. Образовавшийся над жидкостью газ отсосем пипеткой (только не ртом, так как выдыхаемый воздух тоже содержит CO2) и выпустим его во вторую пробирку с известковой водой.
Как мы уже установили, углекислый газ в 1,5 раза тяжелее воздуха. Поэтому его можно “переливать”, как воду, например. Наполним химический стакан углекислым газом, и осторожно, чтобы не “промахнуться”, перельем невидимый газ во второй стакан. Там обнаружим его с помощью пробы лучинкой. Дым от погасшей лучины повиснет в CO2. Можно до переливания. сделать газ видимым. Для этого добавим в стакан с газом две капли концентрированной соляной кислоты и две капли концентрированного гидроксида аммония (нашатырного спирта), затем осторожно перемешаем стеклянной палочкой образовавшийся туман хлорида аммония (нашатыря) с диоксидом углерода. Для забавы можно потушить в нем горящую свечку.
Наполним широкий сосуд (чашку) углекислым газом до половины и будем выдувать мыльные пузыри таким образом, чтобы они с небольшой высоты падали на газ. После нескольких неудачных попыток нам удастся получить мыльный пузырь, который плавает на газе. Раствор для мыльных пузырей приготовим из жидкого мыла, которое смешаем с холодной дистиллированной водой и куда через несколько часов добавим несколько капель пропантриола (глицерина).
Наполним пробирку углекислым газом, вольем 1—2 мл раствора едкой щелочи (гидроксида калия или натрия), тотчас закроем пробирку смоченным большим пальцем и встряхнем ее. (Осторожно! Не разбрызгивать щелочь! Сразу же после опыта вымыть руки!) Пробирка свободно повисает на пальце. Не отнимая пальца, перевернем ее, опустим в воду отверстием вниз и откроем. Вода устремится в пробирку и заполню большую ее часть.
Диоксид углерода взаимодействует со щелочами с образованием карбонатов, в результате в пробирке образуется вакуум. Внешнее давление воздуха прочно прижимает пробирку к пальцу.
Эту реакцию применяют, если необходимо удалить диоксид углерода из газовой смеси. Смесь пропускают через большое количество промывных склянок, наполненных щелочью.
Посмотрим, как газируется вода в сифоне. Насадим баллончик затворной стороной (алюминиевой пластинкой) на острие сапожного гвоздя, обернем тонкой хлопчатобумажной тканью (носовым платком) и сильно ударим молотком по дну патрона. Газ выделится с сильным шипением, белые пары пройдут через поры ткани, а в самом платке останется белый осадок —твердый диоксид углерода, так называемый сухой лед.
Диоксид углерода можно сжижать под давлением при температуре ниже —31,3°С (критическая температура). Жидким СО2 заряжены баллоны. Когда при ударе пробивается затворная пластина, СО2 выходит и испаряется очень быстро. Благодаря работе, производимой при испарении и расширении, газ очень сильно охлаждается, и часть его конденсируется.
Сухой лед нельзя сжимать пальцами (обмораживание кожи!). Остерегайтесь, чтобы ни малейшей крупинки не попало в глаза. При работе снять с рук кольца!
Сухой лед применяется прежде всего для охлаждения пищевых продуктов. Холода от него вдвое больше, чем от обычного льда, а кроме того, он удобен тем, что испаряется без остатка.
У продавца мороженого обычно можно попросить сухой лед и провести с ним несколько интересных опытов.
Наполним бутылку из-под пива или лимонада на четыре пятых фруктовым соком или водой, бросим внутрь кусочек сухого льда, тотчас закроем, подождем несколько минут и затем сильно взболтаем. Получится газированный напиток. (Ни в коем случае не брать много сухого льда, так как бутылка может взорваться; достаточно кусочка величиной с горошину. В целях безопасности обернем бутылку полотенцем.)
Кусочек сухого льда бросим в наполненную на три четверти водой плоскодонную колбу (можно взять молочную бутылку или что-то похожее), затем закроем ее пробкой с отверстием. В отверстие вставим оттянутую на конце стеклянную трубку, которая вплотную доходит до дна сосуда. Вскоре вода будет сильной струёй разбрызгиваться из трубки.
При тушении пожара диоксид углерода часто используют для выброса гасящего средства. Мы можем сделать модель пенного огнетушителя — см. рисунок.
Несколько кусочков сухого льда положим в полотняный мешочек и измельчим ударами молотка. (Надеть защитные очки!) Полученную массу смешаем в фарфоровой чашке с пропиловым спиртом или денатуратом до образования кашицы. В чашку положим кусок резинового шланга, цветок и небольшой плод. Температура охлаждающей смеси примерно —80 °С. Вытащенный резиновый шланг станет твердым и расколется, если по нему ударить молотком. Цветок и плод замерзнут и при падении на твердую поверхность разлетятся вдребезги.
Получение соды
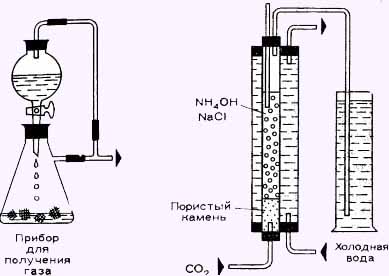 Для этого опыта применим аппарат, в котором при
небольшом давлении получим диоксид углерода
(углекислый газ). Подсоединим к газоотводной
трубке этого аппарата Т-образную трубку, одно
колено которой свяжем с капельной воронкой (см.
рисунок). Диоксид углерода получим при
взаимодействии кусочков мрамора и 20%-ного
раствора соляной кислоты. Чтобы
проконтролировать количество образующегося
газа, подсоединим к газообразователю промывную
склянку, частично наполненную водой. Диоксид
углерода должен проходить через реакционный
сосуд в виде мелких пузырьков. Для этой цели
приобретем в зоологическом магазине не слишком
большой пористый камень, который применяется в
аэрационной установке аквариума *. Напильником
придадим ему круглую форму, чтобы он подошел к
стеклянной трубке, имеющей внутренний диаметр
15—20 мм (трубка для сжигания длиной примерно 30 ем).
Трубку, подводящую газ, приклеим к камню
водостойким клеем. Диаметр ее должен быть не
менее 6 мм. Перед сборкой аппаратуры проверим
проницаемость камня, погружая его в воду и
пропуская через него воздух. Реакционный сосуд
укрепим на штативе. Избыток диоксида углерода
улетучится в воздух через открытую вверху
трубку. Если имеется подходящее оборудование,
можно сделать вокруг реакционного сосуда
охлаждающую рубашку (так как температура при
реакции не должна превышать 30 °С), а реакционный
сосуд закрыть сверху пробкой с двумя
отверстиями, в одном из которых помещается
термометр, а в другом — отводная трубка (как
показано на рисунке). Но можно использовать и
более простую установку.
Для этого опыта применим аппарат, в котором при
небольшом давлении получим диоксид углерода
(углекислый газ). Подсоединим к газоотводной
трубке этого аппарата Т-образную трубку, одно
колено которой свяжем с капельной воронкой (см.
рисунок). Диоксид углерода получим при
взаимодействии кусочков мрамора и 20%-ного
раствора соляной кислоты. Чтобы
проконтролировать количество образующегося
газа, подсоединим к газообразователю промывную
склянку, частично наполненную водой. Диоксид
углерода должен проходить через реакционный
сосуд в виде мелких пузырьков. Для этой цели
приобретем в зоологическом магазине не слишком
большой пористый камень, который применяется в
аэрационной установке аквариума *. Напильником
придадим ему круглую форму, чтобы он подошел к
стеклянной трубке, имеющей внутренний диаметр
15—20 мм (трубка для сжигания длиной примерно 30 ем).
Трубку, подводящую газ, приклеим к камню
водостойким клеем. Диаметр ее должен быть не
менее 6 мм. Перед сборкой аппаратуры проверим
проницаемость камня, погружая его в воду и
пропуская через него воздух. Реакционный сосуд
укрепим на штативе. Избыток диоксида углерода
улетучится в воздух через открытую вверху
трубку. Если имеется подходящее оборудование,
можно сделать вокруг реакционного сосуда
охлаждающую рубашку (так как температура при
реакции не должна превышать 30 °С), а реакционный
сосуд закрыть сверху пробкой с двумя
отверстиями, в одном из которых помещается
термометр, а в другом — отводная трубка (как
показано на рисунке). Но можно использовать и
более простую установку.
Применяя трубку длиной 30 см и диаметром 2 см, мы используем 60 мл реакционного раствора. Его мы можем приготовить двумя путями: или смешав 20 мл концентрированного раствора гидроксида аммония с 40 мл насыщенного раствора поваренной соли (14 г NaCl в 40 мл HgO), или растворив до насыщения поваренную соль в концентрированном растворе гидроксида аммония.
Примерно через 20 мин после начала опыта раствор помутнеет — это началось выделение гидрокарбоната натрия. Теперь необходимо внимательно следить за реакцией в трубе, так как выпадающая соль может закрыть поры в камне. Из-за этого в промывной склянке и газообразователе повысится давление газа. Надо тотчас же отсоединить реакционную трубу и промывную склянку и зажать шланг. Затем приостановим образование Диоксида углерода.
Оставим еще на некоторое время раствор в трубе для охлаждения; выделение гидрокарбоната натрия при этом продолжится. Наконец, отфильтруем и просушим соль, отжав ее между листами фильтровальной бумаги и оставив в умеренна теплом месте. Мы получим более 5 г гидрокарбоната натрия, который необходимо еще кальцинировать. Поместим его в про бирку из термостойкого стекла, закроем ее пробкой со встав ленной газоотводной трубкой и укрепим на штативе. Сначала сильно нагреем гидрокарбонат натрия на пламени горелки. Выделяющийся ,газ соберем в пневматической ванне. Докажем с помощью горящей лучины и взаимодействием с известковой водой, что это диоксид углерода. В пробирке останется карбонат натрия, при взаимодействии которого с разбавленной соляной кислотой выделяется диоксид углерода:
Na2CO3 + 2НС1 = 2NaCl + Н2О + СО2
По способу Сольве аммиак регенерируют, смешивая раствор хлорида аммония с известковым молоком. Добавим в пробирку с несколькими миллилитрами раствора хлорида аммония немного гашеной извести Са(ОН)а, выделяющийся аммиак обнаружим известным способом:
2NH4C1+ Са(ОН)2 = СаСl2 + 2Н2О+ 2NH3
Безводная, или кальцинированная, сода —гигроскопичный белый порошок, который очень хорошо растворяется в чуть, теплой воде. Раствор соды дает щелочную реакцию. Сода получается в кристаллическом виде, если ее осаждать из раствора при температуре ниже 32 °С. Кристаллическая сода имеет формулу Na2CO3-10H2O. Это значит, что при кристаллизации на 1 моль карбоната натрия всегда приходится 10 молей кристаллизационной воды. При длительном хранении прозрачные кристаллы покрываются белым налетом. Благодаря “выветриванию” они теряют воду, и на поверхности остается безводный карбонат натрия.
Поддержите сайт, поставте на нас ссылку. | |
| Пример ссылки | Код ссылки |
| Мир химии | |
| Выбрать другой баннер... | |





