Химия
ОСНОВЫ ТЕОРЕТИЧЕСКОЙ ХИМИИ
8. Растворы электролитов
Электролиты.
Известно, что существуют две основные причины прохождения электрического тока через проводники: либо за счет движения электронов в электрическом поле, либо за счет движения ионов. Электронная проводимость присуща, прежде всего, металлам.Ионная проводимость присуща многим химическим соединениям, обладающим ионным строением, например солям в твердом или расплавленном состояниях, а также многим водным и неводным растворам. В связи с этим все вещества принято условно делить по их поведению в растворах на две категории: а) вещества, растворы которых обладают ионной проводимостью (электролиты); б) вещества, растворы которых не обладают ионной проводимостью (неэлектролиты). К электролитам относится большинство неорганических кислот, оснований и солей. К неэлектролитам относятся многие органические соединения, например спирты, углеводы.
Электролитическая диссоциация. Кроме хорошей электропроводности, растворы электролитов обладают более низкими значениями давления пара растворителя и температуры плавления и более высокими температурами кипения по сравнению с соответствующими значениями для чистого растворителя или для раствора неэлектролита в этом же растворителе. Для объяснения этих свойств шведский ученый С. Аррениус в 1887 г. предложил теорию электролитической диссоциации.
Под электролитической диссоциацией понимается распад молекул электролита в растворе с образованием положительно и отрицательно заряженных ионов — катионов и анионов.
Процесс диссоциации во всех случаях является обратимым, поэтому при написании уравнений реакции диссоциации необходимо применять знак обратимости «
. Различные электролиты, согласно теории Аррениуса, диссоциируют на ионы в различной степени. Полнота распада зависит от природы электролита, его концентрации, природы растворителя, температуры.Степень диссоциации. Одним из важнейших понятий теории электролитической диссоциации Аррениуса является понятие о степени диссоциации.
Степенью диссоциации а называется отношение числа молекул, распавшихся на ионы (n'), к общему числу растворенных молекул (п):
![]()
Из этого выражения очевидно, что а может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация). Степень диссоциации часто выражают в процентах. Степень диссоциации электролита может быть определена только экспериментальным путем, например по измерению температуры замерзания раствора, по электропроводности раствора и т. д.
Сильные и слабые электролиты. В зависимости от степени диссоциации различают электролиты сильные и слабые. Электролиты со степенью диссоциации больше 30% обычно называют сильными, со степенью диссоциации от 3 до 30% — средними, менее 3% — слабыми электролитами.
К сильным электролитам относятся почти все соли, некоторые кислоты (НС
l, HBr, HI, НNО3, НсlO4, Н2SO4(разб.)) и некоторые основания (LiОН, NaOH, КОН, Са(ОН)2, Sr(OH)2, Ва(ОН)2). К слабым электролитам относится большинство кислот (особенно органических) и оснований.Степень диссоциации как сильных, так и слабых электролитов
зависит от концентрации раствора (степень диссоциации тем выше, чем более разбавлен раствор).Константа диссоциации. Более точной характеристикой диссоциации электролита является константа диссоциации, которая от концентрации раствора не зависит.
Выражение для константы диссоциации можно получить, если записать уравнение реакции диссоциации электролита АК в общем виде:
A K « A- + K+.
Поскольку диссоциация является обратимым равновесным процессом, то к этой реакции
применим закон действующих масс, и можно определить константу равновесия как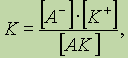
где К — константа диссоциации, которая зависит от температуры и природы электролита и растворителя, но не зависит от концентрации электролита.
Диапазон констант равновесия для разных реакций очень большой — от 10-16 до 1015. Например, высокое значение К для реакции
![]()
означает, что если в раствор, содержащий ионы серебра
Ag+, внести металлическую медь, то в момент достижения равновесия концентрация ионов меди [Cu2+] намного больше, чем квадрат концентрации ионов серебра [Ag+]2. Напротив, низкое значение К в реакции![]()
говорит о том, что к моменту достижения равновесия растворилось ничтожно малое количество иодида серебра
AgI.Обратите особое внимание на форму записи выражений для константы равновесия. Если концентрации некоторых реагентов существенно не изменяются в процессе реакции, то они не записываются в выражение для константы равновесия (такие константы обозначаются К
1).Так, для реакции меди с серебром неправильным будет выражение
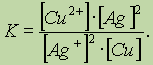
Правильной будет следующая форма записи:
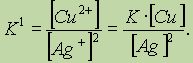
Это объясняется тем, что концентрации металлических меди и серебра введены в константу равновесия. Концентрации меди и серебра определяются их плотностью и не могут быть изменены. Поэтому эти концентрации нет смысла учитывать при расчете константы равновесия.
Аналогично объясняются выражения констант равновесия при растворении
AgCl и AgI.Произведение растворимости.
Константы диссоциации малорастворимых солей и гидроксидов металлов называются произведением растворимости соответствующих веществ (обозначается ПР).Для реакции диссоциации воды
![]()
выражение
константы будет:![]()
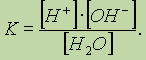
Объясняется это тем, что концентрация воды во время реакций в водных растворах изменяется очень незначительно. Поэтому принимается, что концентрация
[Н2О] остается постоянной и вводится в константу равновесия.Ионные уравнения реакций. Поскольку электролиты в растворах образуют ионы, то для отражения сущности реакций часто используют так называемые ионные уравнения реакций. Написанием ионных уравнений подчеркивается тот факт, что, согласно теории диссоциации, в растворах происходят реакции не между молекулами, а между ионами.
С точки зрения теории диссоциации при реакциях между ионами в растворах электролитов возможны два исхода:
1. Образующиеся вещества — сильные электролиты, хорошо растворимые в воде и полностью диссоциирующие на ионы.
2. Одно (или несколько) из образующихся веществ — газ, осадок или слабый электролит (хорошо растворимый в воде).
Рассмотрим две реакции:
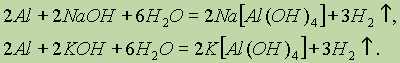
В ионной форме эти уравнения запишутся следующим образом:
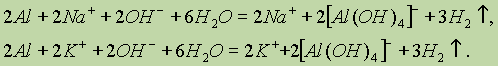
В данном случае алюминий не является электролитом, а молекула воды записывается в недиссоциированной форме потому, что является очень слабым электролитом. Неполярные молекулы водорода практически нерастворимы в воде и удаляются из сферы реакции. Одинаковые ионы в обеих частях уравнений
можно сократить, и тогда эти уравнения преобразуются в одно сокращенное ионное уравнение взаимодействия алюминия с щелочами:![]()
Очевидно, что при взаимодействии алюминия с любой щелочью реакция будет описываться уравнением
Следовательно, ионное уравнение, в отличие от молекулярного, относится не к одной какой-нибудь реакции между конкретными веществами, а к целой группе аналогичных реакций. В этом его большая практическая ценность и значение, например благодаря этому широко используются качественные реакции на различные ионы.С учетом вышеизложенного можно сформулировать правило, которым удобно руководствоваться при изучении процессов, протекающих в растворах электролитов.
Реакции между ионами в растворах электролитов идут практически до конца в сторону образования осадков, газов и слабых электролитов.
Следовательно, реакции идут с образованием веществ с меньшей концентрацией ионов в растворе в соответствии с законом действующих масс. Скорость прямой реакции пропорциональна произведению концентраций ионов реагирующих компонентов, а скорость обратной реакции пропорциональна произведению концентраций ионов продуктов. Но при образовании газов, осадков и слабых электролитов ионы связываются (уходят из раствора) и скорость обратной реакции уменьшается.
Ионное произведение воды. Константа воды
При диссоциации воды (см. уравнение выше) на каждый ион Н
+ образуется один ион ОН- , следовательно, в чистой воде концентрации этих ионов должны быть одинаковы: [H+] = [ОН- ]. Используя значение ионного произведения воды, находим:![]()
Такова концентрация ионов Н
+ и ОН- в чистой воде. Рассмотрим, как изменится концентрация при добавлении других веществ, например соляной кислоты. Соляная кислота — сильный электролит, диссоциирующий в воде на ионы H+ и Cl- . Следовательно, концентрация ионов Н+ в растворе будет увеличиваться. Однако ионное произведение воды от концентрации не зависит, поэтому при увеличении [Н+] должна уменьшаться [ОН- ].Напротив, если к воде добавить щелочь, то концентрация [ОН- ] увеличится, а
[Н+] уменьшится. Таким образом, концентрации [Н+] и [ОН- ] взаимосвязаны: чем больше одна величина, тем меньше другая, и наоборот.Кислотность растворов обычно выражают через концентрацию ионов Н
+. В кислых растворах [Н+]>10-7 моль/л, в нейтральных [Н+] = 10-7 моль/л, в щелочных [Н+]< 10-7 моль/л.рН раствора. Чтобы не писать числа с показателем степени, кислотность раствора часто выражают через отрицательный логарифм концентрации ионов водорода, называя эту величину водородным показателем и обозначая ее рН:
![]()
В кислых растворах рН < 7, в нейтральных рН = 7, в щелочных рН > 7.
Основные классы неорганических веществ:
а) Оксиды. Оксидами называются сложные вещества, состоящие из двух элементов, один из которых кислород.
Почти все химические элементы образуют оксиды. До настоящего времени еще не получены оксиды трех элементов — благородных газов гелия, неона и аргона.
Согласно международной номенклатуре названия оксидов образуют из латинского корня названия элемента с большей относительной электроотрицательностью с окончанием -ид и русского названия элемента с меньшей относительной электроотрицательностью в родительном падеже. Если же элемент образует несколько оксидов, то в их названиях указывается степень окисления элемента римской цифрой в скобках сразу после названия. Например, Н2О — оксид водорода (вода), FeО — оксид железа (II), Fe2O3 — оксид железа (III), Р2O3 — оксид фосфора (III), Р2О5 — оксид фосфора (V), P4O6 — гексаоксид тетра-фосфора, Р4O10 — декаоксид тетрафосфора, Сu2О — оксид меди (I) или оксид димеди.
Особую группу кислородных соединений элементов составляют пероксиды. Обычно их рассматривают как соли пероксида водорода Н2O2, проявляющего слабые кислотные свойства. У пероксидов атомы кислорода химически связаны не только с атомами других элементов, но и между собой (образуют пероксидную группу —О—О—. Например, пероксид натрия Na2О2 (пероксо- — название группы —О—О—). Надо уметь правильно определять степень окисления элементов в пероксидах. Так, в пероксиде бария ВаO2 степень окисления бария равна +2, а кислорода -1.
По химическим свойствам оксиды делятся на три группы: основные, кислотные и амфотерные.
Основные оксиды. Основными называются такие оксиды, которым соответствуют основания. Например, Nа2O, СаО, FеО, NiO являются основными оксидами, так как им соответствуют основания NаОН, Са(ОН)2, Fе(ОН)2, Ni(ОН)2. Некоторые основные оксиды при взаимодействии с водой образуют основания:
![]()
Другие основные оксиды непосредственно с водой не взаимодействуют, а соответствующие им основания получаются из солей:
![]()
Основные оксиды образуются только металлами.
Кислотные оксиды.
Кислотными оксидами называются такие оксиды, которым соответствуют кислоты. Например, СО2, P2O5, SO2, SO3 — кислотные оксиды, так как им соответствуют кислоты H2CO3, H3PO4, H2SO3, H2SO4. Большинство кислотных оксидов образуют кислоты при взаимодействии с водой:![]()
Некоторые же кислотные оксиды с водой не взаимодействуют. Однако сами они могут быть получены из соответствующей кислоты:
![]()
Кислотные оксиды образуются неметаллами и некоторыми металлами, проявляющими высокие степени окисления (например, оксиду
Mn2О7, отвечает марганцовая кислота НMnO4).Амфотерные оксиды.
Амфотерными называются такие оксиды, которые в зависимости от условий проявляют основные или кислотные свойства, т.е. обладают двойственными свойствами. К ним относятся некоторые оксиды металлов: ZnO, Аl2O3, Cr2O3 и др. Амфотерные оксиды с водой непосредственно не соединяются, но они реагируют и с кислотами, и с основаниями: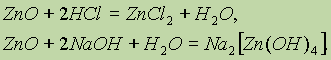
При сплавлении А
2O3 со щелочами или карбонатами щелочных металлов образуются метаалюминаты (безводные алюминаты):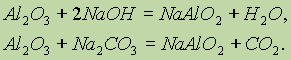
Основные, кислотные и амфотерные оксиды являются солеобразующими, т.е. обладают способностью образовывать соли (при взаимодействии с кислотами или основаниями). Имеется небольшая группа оксидов, которые не проявляют ни основных, ни кислотных свойств и не образуют солей Такие оксиды называются безразличными или индифферентными. К ним, например, относятся оксид углерода (
II) СО, оксид азота (I) N2O, оксид азота (II) NO и оксид кремния (II)SiO.Кислоты, соли и основания в свете теории диссоциации электролитов.
Определения кислот, солей и оснований с точки зрения теории диссоциации были даны С. Аррениусом.б) Кислоты. Кислотой называется соединение, образующее при диссоциации в водном растворе из положительных ионов только ионы водорода Н+. В соответствии с этими определениями к кислотам относятся, например, НСl, H2SO4, HNO3, H2S.
Примеры уравнений диссоциации кислот можно записать с учетом гидратации ионов:
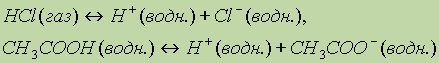
Числом ионов водорода, образуемых каждой молекулой кислоты при диссоциации, определяется заряд кислотного остатка (аниона). Соляная и азотная кислоты образуют только однозарядные кислотные остатки (С
l- ,NО3-); молекула серной кислоты (Н2SO4 может образовать два кислотных остатка: однозарядный (НSO4-) и двухзарядный (SO42-); молекула фосфорной кислоты может дать три кислотных остатка: однозарядный, двухзарядный и трехзарядный (Н2РО4-, НРО42- и РО43-).Различают кислородные и бескислородные кислоты. Как показывает само название, первые содержат кислород (например Н
2SO4, НNO3, Н3РО4), вторые его не содержат (например, НСl, НВr, НI, H2S).Названия кислородных кислот производятся от названия неметалла с прибавлением окончаний -ная, -вая, если степень окисления его соответствует номеру группы. По мере понижения степени окисления суффиксы меняются в следующем порядке: -оватая, -истая, -оватистая.
Если элемент в одной и той же степени окисления образует несколько кислородсодержащих кислот, то к названию кислоты с меньшим содержанием кислородных атомов добавляется префикс “мета”,
при наибольшем числе — префикс “орто”.Названия бескислородных кислот производятся от названия неметалла с окончанием -о и прибавлением слова водородная.
в) Основания.
Основанием называется соединение, образующее при диссоциации в водном растворе из отрицательных ионов только гидроксид-ионы ОН- . В соответствии с этими определениями к основаниям относятся, например, NaOH, Са(ОН)2, NH4OH.Диссоциацию оснований с учетом гидратации ионов следует писать так:
![]()
Согласно международной номенклатуре названия оснований составляются из слова гидроксид и названия металла. Например, NаОН — гидроксид натрия, КОН — гидроксид калия, Са(ОН)
2 — гидроксид кальция. Если элемент образует несколько оснований, то в названиях указывается степень его окисления римской цифрой в скобках: Fe(ОН)2 — гидроксид железа (II), Fе(ОН)3 — гидроксид железа (III).Помимо этих названий, для некоторых наиболее важных оснований применяются и другие, в основном традиционные русские названия. Например, гидроксид натрия
NаОН называют едкий натр; гидроксид калия КОН — едкое кали; гидроксид кальция Са(ОН)2 — гашеная известь; гидроксид бария Ва(ОН)2 — едкий барит.Амфотерные гидроксиды.
Амфотерными называются такие гидроксиды, которые при диссоциации образуют одновременно и катионы водорода Н+, и гидроксид-ионы ОН-. Такими являются Аl(ОН)3, Zn(ОН)2, Сr(ОН)3, Ве(ОН)2, Gе(ОН)2, Sn(ОН)4, Рb(ОН)2 и др.Амфотерные гидроксиды взаимодействуют как с растворами кислот, так и с растворами щелочей:
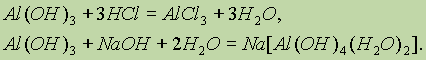
В настоящее время растворение амфотерных гидроксидов в щелочных растворах обычно рассматривается как процесс образования гидроксосолей (гидроксокомплексов). Экспериментально доказано существование гидроксокомплексов многих металлов: [
Zn(OH)4]2-, [Al(OH)4(H2O)2]-, [Al(OH)6]3- и т.д. Наиболее прочны гидроксокомплексы алюминия, а из них —[Al(OH)4(H2O)2]-.Такой подход не меняет сделанных выводов: у амфотерного гидроксида, например у А1(ОН)
3 и ему подобных, в кислой среде равновесие смещается в сторону образования солей алюминия, в щелочной — в сторону образования гидроксокомплексов. Очевидно, в водном растворе существует равновесие, которое более точно описывается уравнением: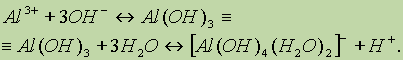
г)
Cоли. Солями называются соединения, образующие при диссоциации в водном растворе положительно заряженные ионы металлов и отрицательно заряженные ионы кислотных остатков, а иногда, кроме них, ионы водорода и гидроксид-ионы: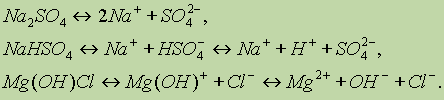
В соответствии с данным определением соли делятся на средние
(Na2SO4), кислые (NaHSO4) и основные (Mg(OH)Cl).После Аррениуса было показано, что определение кислот, солей и оснований в терминах теории электролитической диссоциации не охватывает всего многообразия кислотно-основных свойств веществ.
Так, например, в рамки приведенных определений не укладываются соли
NH4Cl и хлорид фениламмония C6H5NH3Cl, основание NH3 и др.Уравнения диссоциации солей, с учетом гидратации ионов, следует записывать так:
![]()
Любую соль можно представить как продукт взаимодействия основания и кислоты, т.е. реакции нейтрализации:
![]()
Уравнение диссоциации средней соли
Na2SO4 можно записать так:![]()
Если основания взято меньше, чем требуется для полной нейтрализации серной кислоты, то при
упаривании будут выпадать кристаллы кислой соли:![]()
Диссоциацию кислой соли можно выразить уравнением:
![]()
Анион кислой соли подвергается вторичной диссоциации как слабый электролит:
![]()
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют.
Основные соли можно представить как продукт неполного замещения гидроксогрупп основания на кислотные остатки
:![]()
Диссоциацию основной соли можно выразить уравнением
![]()
Катион основной соли в незначительной степени подвергается дальнейшей диссоциации:
![]()
Двойные соли состоят из ионов двух разных металлов и кислотного остатка.
Например, КАl(SO4)2, (NН4)2Fe(SO4)2. Диссоциацию таких солей можно выразить уравнениями:![]()
Двойные соли диссоциируют на ионы металлов и кислотного остатка.
В состав комплексных солей входят сложные (комплексные) ионы (в формулах они заключаются в квадратные скобки), которые и отщепляются при диссоциации:
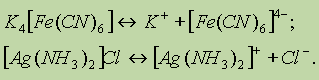
В свою очередь сложные (комплексные) ионы в очень малой степени подвергаются дальнейшей диссоциации:
![]()
Таким образом, комплексные соли при диссоциации сначала отщепляют комплексные ионы, которые затем подвергаются вторичной диссоциации как слабые электролиты.
Наиболее распространены международные названия солей. Они состоят из двух слов: название аниона в именительном падеже и катиона в родительном. Число анионов и катионов, как правило, не указывается. Но если один и тот же металл проявляет различную степень окисления, то ее указывают в скобках римской цифрой. Например, К
NO3 — нитрат калия, FeSO4 — сульфат железа (II), Fe2(SO4)3 — сульфат железа (III), NaС1 — хлорид натрия.Названия кислых солей образуются добавлением к аниону приставки гидро-, а если необходимо, то с соответствующими числительными: NаН
SO4 — гидросульфат натрия; КН2PO4 — дигидрофосфат калия. Названия основных солей образуют, добавляя к наименованию аниона соответствующей средней соли приставки “гидроксо”: Аl(ОН)SO4 — гидроксосульфат алюминия, А1(ОН)2Cl — дигидроксохлорид алюминия.Гидролиз солей.
Реакция чистой воды является нейтральной (рН = 7). Водные растворы кислот и оснований имеют соответственно кислую (рН < 7) и щелочную (рН > 7) реакцию. Практика, однако, показывает, что не только кислоты и основания, но и соли могут иметь щелочную или кислую реакцию — причиной этого является гидролиз солей.Взаимодействие солей с водой, в результате которого образуются кислота (или кислая соль) и основание (или основная соль), называется гидролизом солей.
Причиной гидролиза является электролитическая диссоциация соответствующих солей и воды. Вода незначительно диссоциирует на ионы Н+ и ОН- , но в процессе гидролиза один или оба из этих ионов могут связываться ионами, образующимися при диссоциации соли, в малодиссоциированные, летучие или труднорастворимые вещества. Рассмотрим гидролиз солей следующих основных типов:
1.
Соли сильного основания и сильной кислоты, при растворении в воде (например, NaCI, CaCl2, К2SO4) не гидролизуются, и раствор соли имеет нейтральную реакцию.2.
Соли сильного основания и слабой кислоты, например КСlO, Na2CO3, СН3СООNа, NaCN, Na2S, К2SiO3. Запишем уравнение гидролиза ацетата натрия:![]()
В результате реакции образовался слабый электролит — уксусная кислота. В ионном виде этот процесс можно записать так:
![]()
Следовательно, раствор СН
3СООNа будет проявлять щелочную реакцию.При растворении солей многоосновных кислот гидролиз протекает ступенчато, например:
![]()
или в ионной форме
![]()
Этот процесс
отражает гидролиз Na2S по первой ступени. Чтобы гидролиз прошел полностью, как правило, увеличивают температуру процесса:![]()
Таким образом, при растворении в воде соли сильного основания и слабой кислоты раствор приобретает щелочную реакцию вследствие гидролиза.
3.
Соли слабого основания и сильной кислоты, например Аl2(SO4)3, FeCl2, CuBr2, NH4Cl.Рассмотрим гидролиз хлорида железа
(II):![]()
В ионном виде этот процесс можно записать так:
![]()
По второй ступени гидролиз протекает следующим образом:
![]()
Из приведенных реакций ясно, что в результате гидролиза солей слабого основания и сильной кислоты раствор приобретает кислую реакцию.
4.
Соли слабого основания и слабой кислоты, например Al2S3, Сr2S3, СНзСООNН4, (NH4)CO3. При растворении в воде таких солей образуются малодиссоциирующие кислота и основание:![]()
или в ионном виде:
![]()
Реакция среды в растворах подобных солей зависит от относительной силы кислоты и основания.
Другими словами, водные растворы таких солей могут иметь нейтральную, кислую или щелочную реакцию в зависимости от констант диссоциации образующихся кислот и оснований.Так, при гидролизе СН3СООNН4 реакция раствора будет слабощелочной, поскольку константа диссоциации гидроксида аммония (К = 6,3× 10- 5) больше константы диссоциации уксусной кислоты (К = 1,75× 10- 5).
Протонные кислоты.
Электролитическая диссоциация явилась основой успешного развития теории растворов и изучения процессов, протекающих в них. В этом заключается ее большое значение в химии. Однако эта теория не объясняет процессов, протекающих в неводных растворах. Так, например, если хлорид аммония в водном растворе ведет себя как соль (диссоциирует на ионы NН4+ и Сl- ), то в жидком аммиаке он проявляет свойства кислоты, — растворяет металлы с выделением водорода. Как основание ведет себя азотная кислота, растворенная в жидком фтороводороде или в безводной серной кислоте. Эти факты не согласуются с теорией электролитической диссоциации. Их объясняет протолитическая теория кислот и оснований, предложенная в 1923 г. независимо датским ученым Бренстедом и английским ученым Лоури. Согласно этой теории кислотами являются вещества, молекулы или ионы, отщепляющие при данной реакции протоны. Основаниями являются вещества, молекулы или ионы, присоединяющие протоны. Как те, так и другие получили общее название протолитов.Реакция отщепления протона изображается уравнением:
кислота « основание + Н
+Кислота и основание такого процесса называется сопряженными.
Это кислотно-основная пара. Например, ион H3О+ — кислота, сопряженная основанию H2O, а хлорид-ион Cl- — основание, сопряженное кислоте HCI.Свободные протоны в растворах самостоятельно не существуют. Они переходят от кислоты к какому-либо основанию. Поэтому в растворе всегда протекают два процесса:
кислота
1 « основание1 + Н+основание
2 + Н+ « кислота2и равновесие между ними изображают уравнением
кислота
1 + основание2 « основание1 + кислота2Например, реакцию нейтрализации уксусной кислоты аммиаком можно представить так:
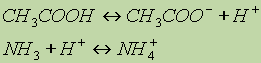
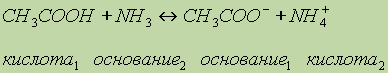
Здесь уксусная кислота является кислотой (отдает протоны Н
+), аммиак — основанием (принимает протоны), ионы СН3СОО- играют роль основания (в этом обратимом процессе они могут принять протоны и превратиться обратно в уксусную кислоту), а ионы аммония NH4+ играют роль кислоты (могут отдать протоны).Аналогично можно изобразить проявление основных свойств азотной кислоты, растворенной в жидком фтороводороде:
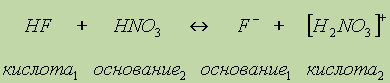
Таким образом, из кислоты и основания всегда получаются новые сопряженные кислота и основание.
Протолитическая теория рассматривает реакцию нейтрализации как переход протона кислоты к основанию.Протолитическая теория расширила круг кислот и оснований по сравнению с представлениями теории электролитической диссоциации: ими могут быть и ионы. Одно и то же вещество а зависимости от того, с чем оно реагирует, может быть или кислотой, или основанием. Теория вскрыла относительность понятий о кислотах и основаниях и показала, что продукты их взаимодействия следует рассматривать как новые кислоты и основания. Протолитическая теория является современной и более общей теорией кислот и оснований.
Кислоты Льюиса. Еще более общее определение кислот и оснований предложил Г. Льюис. Он предположил, что кислотно-основные взаимодействия совсем необязательно происходят с переносом протона. В определении кислот и оснований по Льюису основная роль отводится участию электронных пар в химическом взаимодействии.
Катионы, анионы или нейтральные молекулы, способные принять одну или несколько пар электронов, называют кислотами Льюиса.
Например, фторид алюминия АlF3 — кислота, способная принимать электронную пару при взаимодействии с аммиаком:
AlF3 + : NH3 « [AlF3]: [NH3]
Катионы, анионы или нейтральные молекулы, способные отдавать электронные пары, называют основаниями Льюиса.
Так, согласно определению, аммиак является основанием Льюиса в реакции
![]()
Определение Г. Льюиса охватывает все кислотно-основные процессы, рассмотренные ранее предложенными теориями.
| Вернуться в главное меню | |
|
Если Вам нужно решить задачи по химии, выполнить контрольную работу, написать реферат..., то Вам сюда |
Опыты для дома Химические опыты дома. Всем юным химикам рекомендуется. |
Поддержите сайт, поставте на нас ссылку. | |
| Пример ссылки | Код ссылки |
| Мир химии | |
| Выбрать другой баннер... | |




