Химия
НЕОРГАНИЧЕСКАЯ ХИМИЯ. ЭЛЕМЕНТЫ И ИХ СОЕДИНЕНИЯ
17. Марганец
Свойства элементов
VII B группы.|
Свойства |
25 Mn |
43 Tc |
75 Re |
|
Атомная масса |
54,938 |
99 |
186,21 |
|
Электронная конфигурация* |
|
|
|
|
|
0,126 |
0,136 |
0,137 |
|
|
0,743 |
0,728 |
0,787 |
|
Энергия ионизации
|
7,43 |
7,28 |
7,87 |
|
Относительная электроотрицательность |
1,6 |
- |
1,46 |
|
Возможные степени окисления |
+2, +4, +6, +7 |
+4, +5, +7 |
+2, +4, +6, +7 |
|
кларк, ат.% (распространненость в природе) |
0,03 |
- |
9×10-9 |
|
Агрегатное состояние (н. у.) |
Т В Е Р Д Ы Е В Е Щ Е С Т В А |
||
|
Цвет |
Серебристый |
серебристо-коричневый |
серебристо-белый |
|
|
1245 |
2200 |
3180 |
|
|
2120 |
4600 |
5625 |
|
Плотность |
7,4 |
14,49 |
21,04 |
*Приведены конфигурации внешних электронных уровней атомов соответствующих элементов. Конфигурации остальных электронных уровней совпадают с таковыми для благородных газов, завершающих предыдущий период и указанных в скобках.
Марганец.
Металлический марганец реагирует с кислотами, образуя соли марганца (II):![]()
В различных соединениях марганец проявляет степени окисления 2+, 4+, 6+ и 7+. Чем выше степень окисления, тем более ковалентный характер имеют соответствующие соединения. С возрастанием степени окисления марганца увеличивается также кислотность его оксидов.
При нагревании марганец взаимодействует с кислородом, галогенами, углеродом, бором, кремнием, серой. При взаимодействии марганца с кислородом образуются смешанные оксиды:
![]()
Диспергированный марганец при нагревании реагирует с водой:
![]()
Одной из особенностей марганца является способность поглощать кислород.
Марганец пассивируется в обычных условиях концентрированными кислотами окислителями, хотя при нагревании реакция идет:
![]()
При взаимодействии с разбавленными кислотами выделяется водород:
![]()
На самом деле в растворе существует аквакомплекс
[Mn(H2O)6]Cl2.Марганец взаимодействует со щелочами в присутствие окислителя:
![]()
Оксид марганца (
II). Оксид марганца (II) можно получить восстановление оксида марганца (IV):![]()
Этот оксид обладает основными свойствами. Так, он не реагирует с водой, а при взаимодействии с кислотами образуются соли марганца (
II):![]()
Гидроксид марганца (
II). При взаимодействии солей марганца (II) со щелочами выпадает белый, нерастворимый осадок Mn(OH)2:![]()
При взаимодействии с ки
cлотами от дает соли марганца (II):![]()
При стоянии на воздухе гидроксид марганца (
II) переходит в оксогидроксид, который далее окисляется до оксида марганца (IV):
Аналогичная реакция протекает с сульфидом марганца MnS, но с выпадением осадка серы.
Соли марганца (II). Марганец (II) при взаимодействии с сильными окислителями переходит в различные степени окисления в зависимости от реакции среды:
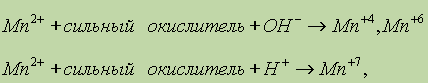
что можно проиллюстрировать следующими примерами:
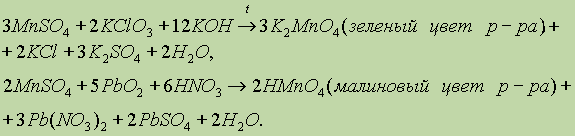
Оксид марганца (
IV). Наиболее важным соединением марганца (IV) является его оксид MnO2. Это соединение коричнево-черного цвета не растворяется в воде. Оксид марганца (IV) — сильный окислитель, который, например, окисляет концентрированную соляную кислоту до хлора:![]()
Эта реакция часто используется для получения хлора в лаборатории.
Этот оксид обладает амфотерными свойствами, равно как и оксогидроксид
MnO(OH)2 и гидроксид Mn(OH)4 марганца (IV):![]()
Манганат калия.
Соединения марганца (VI) малоустойчивы, однако наиболее известное соединение — манганат калия K2MnО4 — устойчив в щелочной среде. Он образуется при восстановлении перманганата калия в щелочной среде, например:![]()
Вообще для
Mn6+ характерны следующие продукты окислительно-восстановительных реакций: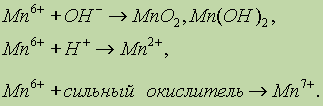
Например:
Перманганат калия.
Высшую степень окисления 7+ марганец имеет в кислотном оксиде Мn2О7 и перманганате калия КмnO4. Последнее вещество — кристаллы фиолетового цвета, хорошо растворимые в воде.Перманганат калия — сильнейший окислитель.
В кислой среде он восстанавливается до ионов Мn2+:![]()
в щелочной
среде — до К2МnO4 (см. выше), а в нейтральной среде — до MnO2: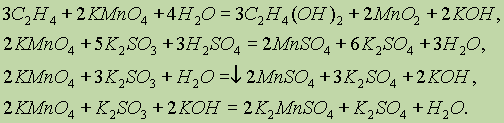
| Вернуться в главное меню | |
|
Если Вам нужно решить задачи по химии, выполнить контрольную работу, написать реферат..., то Вам сюда |
Опыты для дома Химические опыты дома. Всем юным химикам рекомендуется. |
Поддержите сайт, поставте на нас ссылку. | |
| Пример ссылки | Код ссылки |
| Мир химии | |
| Выбрать другой баннер... | |




